新基以2400万美元预付款获下一代肿瘤免疫疗法许可,同款NK技术平台曾获默沙东6.95亿美元合作
2018年12月14日Celgene公司以总计2400万美元的预付款、未来的里程碑和特许权使用费,获得Dragonfly Therapeutics的2种TriNKET™免疫治疗候选药物的授权许可,这次许可代表了两家公司2017年6月合作中的四个血液肿瘤项目中的前两个。
合作历程
2017年6月
Dragonfly Therapeutics和Celgene公司曾签订了预付款为3300万美元的合作协议,共同进行多达4个血液肿瘤候选药物的研发。
2018年11月
双方签订了一项扩大战略性合作协议,使Celgene可以选择获得总共8个肿瘤免疫疗法的独家全球知识产权,并且新增的4个候选药物将研发范围扩展到实体瘤治疗。
作为回报,Celgene已经同意向Dragonfly支付5000万美元的预付款,以及未指明的实现里程碑和特许权使用费相关的未公开支付金额。
候选药物在双方的合作关系首次公布后不到18个月就被成功移交至Celgene,这证实了Dragonfly的研发速度。与最近宣布的其他交易相结合,为Dragonfly建立了一个非常强大的资本状况,而暂时不用出售任何股票。
Celgene商业发展和全球联盟负责人Robert Hershberg博士说道:“Celgene对这些首批TriNKET候选药物的潜力感到兴奋,虽然在完全临床验证之前没有新的机制可以被证实,但我们很高兴这些TriNKET候选药物为患者提供免疫治疗的机会。”
Dragonfly首席执行官(CEO )Bill Haney说:“我们很高兴将2个非常有前途的TriNKET候选药物交给Celgene,并且看到他们推动候选药物向前发展。在过去的18个月里,Celgene团队一直是我们很好的合作伙伴,期待我们继续努力为癌症患者提供潜在的新型肿瘤免疫治疗方案。”
丨Dragonfly与默沙东达成6.95亿美元合作
除了与Celgene的合作关系外,今年10月1日,Dragonfly Therapeutics宣布与默沙东公司达成了一项高达6.95亿美元的许可协议,默沙东将可以获得使用TriNKET™平台开发的一系列实体瘤项目的专有权。双方既没有公开项目的数量,也没有公开实体瘤的类型。
Dragonfly公司开发的肿瘤免疫疗法以专有的三特异性NK细胞衔接蛋白疗法(Tri-specific, NK cell Engager Therapies),即TriNKET™技术为中心,这是一种将自然杀伤(NK)细胞与癌细胞表面蛋白质相连的结合机制。
他们认为,这种方法可以创造出有效的下一代免疫疗法,极大增强免疫疗法的适用范围与疗效,对于像默沙东这样 - 已经在PD-1免疫疗法的尝到甜头但面临瓶颈的公司来说,这可能极具吸引力。随着肿瘤免疫疗法的开发进一步升温,NK细胞在过去几年中已成为癌症研发领域的热门目标,其重要性日益增加。
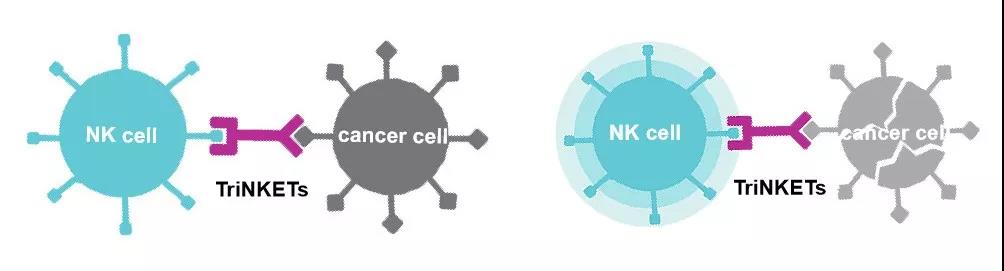

TriNKET作用机制(图片来源:Dragonfly)
通过这种结合,TriNKET旨在刺激NK细胞,唤醒它们意识到癌症,直接杀死肿瘤细胞。此外,TriNKET通过充当哨兵调用其他免疫系统细胞,激活B细胞产生抗肿瘤抗体,并且激活更多的T细胞杀死肿瘤细胞进而放大T细胞的抗癌效力,还可以通过利用它们区分癌症的特殊特征来扩大治疗窗,从而更具体地靶向肿瘤细胞。
目前,Dragonfly的研发管线由六个正在进行的临床前研发项目组成:
-
靶向实体瘤:DF1001
-
靶向血液肿瘤:DF2001、DF3001、DF4001和DF5001
-
以及,TriNKET增强剂:DF6000
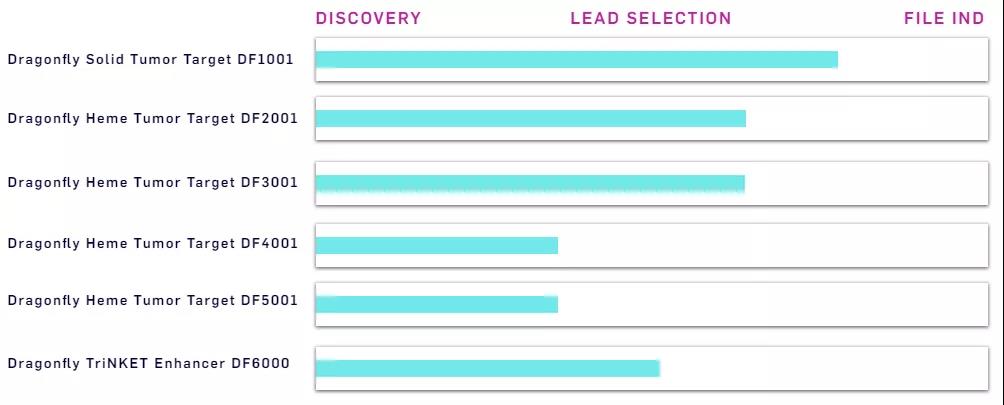
研发管线(图片来源:Dragonfly)
事实上,Dragonfly正在与一些合作伙伴进行积极讨论,以便制定针对新目标的TriNKET疗法,以及寻求加快推进候选药物明年第二季度IND申请的合作。
Celgene
巩固肿瘤免疫疗法的研发管线
早在今年1月,Celgene就已经和CAR-T细胞疗法先驱公司Juno Therapeutics达成协议,拟以90亿美元完成对后者的收购。Juno具有广泛而新颖的产品组合,有望针对多种靶点,对多类癌症进行治疗。3月7日,Celgene宣布完成对Juno Therapeutics的收购,Celgene正式成为肿瘤免疫疗法领域的领军企业之一。
- JCAR017(lisocabtagene maraleucel, liso-cel)是Juno开发的一款靶向CD19 CAR-T细胞疗法,正在进行针对弥漫性/难治性弥漫性大B细胞淋巴瘤(DLBCL)和复发/难治性慢性淋巴细胞白血病(R/R CLL)等血液肿瘤的临床试验。
对比已经上市的Kymriah和Yescarta,JCAR017在治疗DLBCL上表现出极大的竞争力,而且安全风险较小,超一半的临床患者没有出现细胞因子释放综合征(CRS)或神经毒性,有望成为治疗DLBCL的best-in-class疗法。
- JCARH125是Juno开发一款的靶向BCMA CAR-T细胞疗法,用于治疗复发/难治性多发性骨髓瘤(R/R MM)。根据本月初在ASH年会上公布的数据,最低剂量的 CAR-T细胞水平下,ORR为79%,43%的患者达到严格的完全缓解(sCR)或完全缓解(CR)。
此外,Celgene还与bluebird bio联合开发新一代靶向BCMA CAR-T细胞疗法bb21217,用于治疗复发/难治性多发性骨髓瘤(R/R MM)。根据本月初在ASH年会上公布的数据,ORR为83%(n = 10),10名患者中有9名正在进行缓解,其中3名患者完全缓解(CR)或严格完全缓解(sCR),2名患者非常好的部分缓解(VGPR),4名患者部分缓解(PR)。
去年7月,Celgene和百济神州达成战略合作,共同开发和商业化PD-1抑制剂 BGB-A317,用于治疗实体瘤,该合作将涵盖美国、欧洲、日本和亚洲以外的多个国家和地区。
最近宣布与Dragonfly扩大的协议,证明Celgene同时关注血液肿瘤和实体瘤的免疫疗法,进一步延续已有的成果。
